2020年初,一场突如其来的传染病大流行给全世界带来了巨大变数,随后国际病毒分类委员会冠状病毒研究小组(Coronavirus study group)正式命名新型冠状病毒(2019-nCoV)为严重急性呼吸综合征冠状病毒2(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2),这表明新型冠状病毒从分类学角度讲,是SARS冠状病毒(SARS-CoV)的近亲,与2003年“非典”的罪魁祸首SARS病毒部分结构相似,但新型冠状病毒(SARS-CoV-2)具有更强的传染能力和应对温度变化的能力,并且可在复制过程中不断适应宿主而产生突变。在此情况下,人类把终结这一疫情大流行的希望寄托于疫苗的成功研发,各国医疗机构、企业纷纷投入疫苗的研制中。
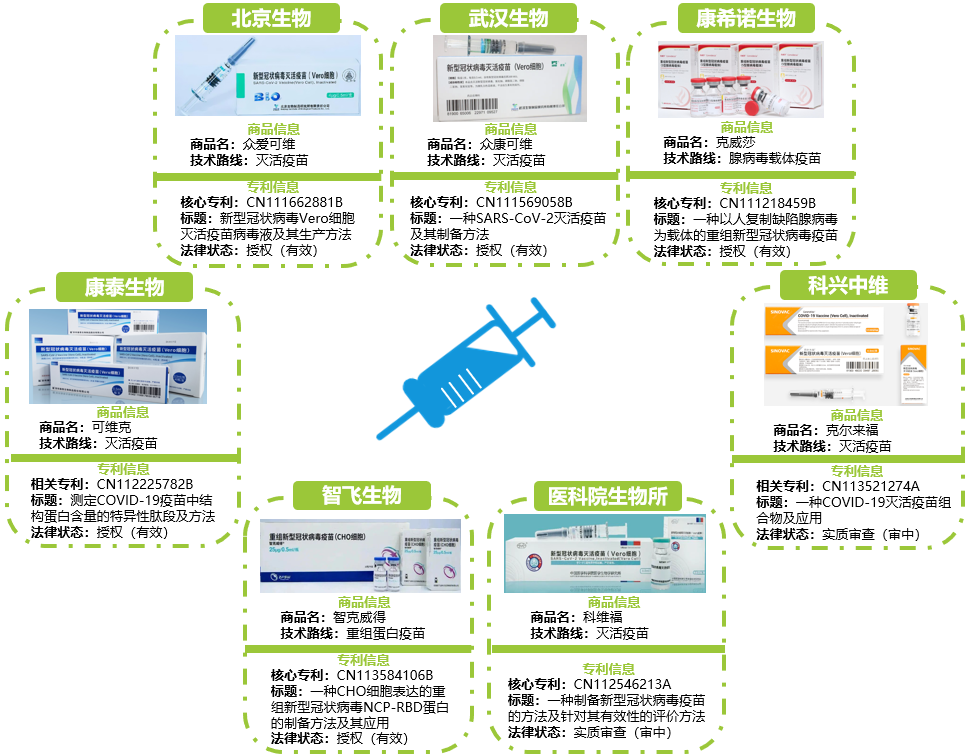
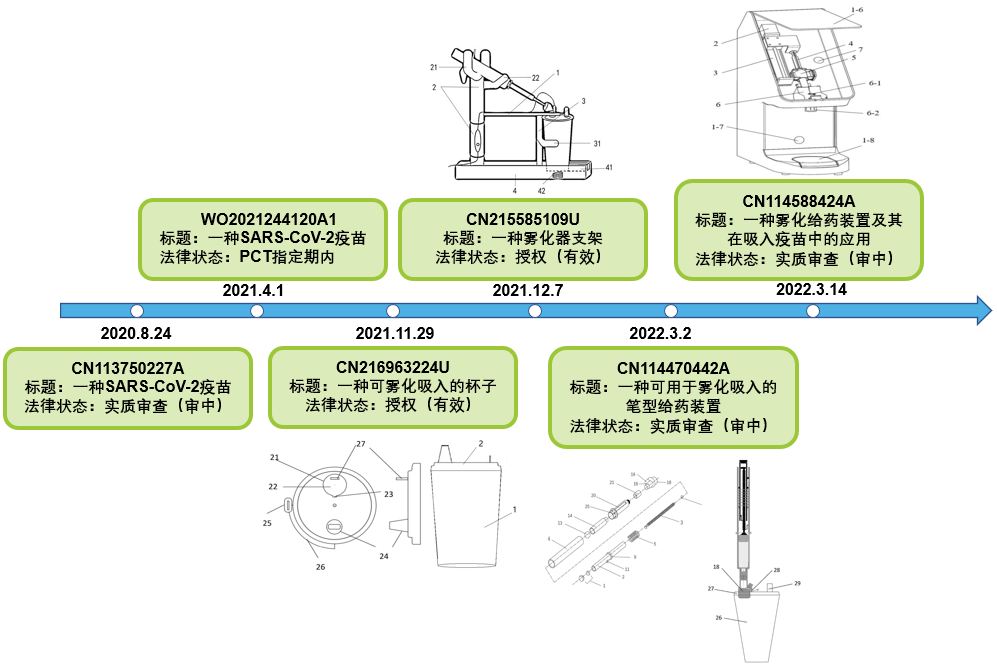
从技术路线上看,新冠疫苗的种类包括灭活疫苗、重组蛋白疫苗、载体疫苗(包括腺病毒载体、减毒流感病毒载体)、核酸疫苗(mRNA疫苗、DNA疫苗)。如图1所示,目前,国内已上市7款新冠疫苗产品,所属单位分别是北京生物、武汉生物、科兴中维、康希诺、智飞生物、康泰生物及中国医学科学院医学生物学研究所(以下简称:医科院生物所),技术路线集中在灭活、重组蛋白及腺病毒载体疫苗。上述企业针对各自在国内上市的新冠疫苗均布局了相关专利(如图1所示),但布局侧重点不同。其中,北京生物、武汉生物、医科院生物所采用的技术路线为灭活疫苗,康希诺生物采用的技术路线为腺病毒载体疫苗,智飞生物采用的技术路线为重组蛋白疫苗,上述企业均布局了疫苗制备方法相关核心专利(CN111662881B、CN111569058B、CN112546213A、CN111218459B、CN113584106B)。而同样采用灭活疫苗技术路线的康泰生物,其全资子公司北京民海生物科技有限公司和科兴中维则从疫苗中结构蛋白含量检测及灭活疫苗组合物方面布局了相关专利(CN112225782B、CN113521274A)。接下来笔者将结合相关专利信息对国内已上市新冠疫苗涉及到的三种技术路线:灭活疫苗、腺病毒载体疫苗、重组蛋白疫苗,以及国内未来新冠疫苗相关技术的研发热点mRNA疫苗作详细介绍。灭活疫苗的原理很简单,就是把经过灭活的病毒,作为抗原,制成疫苗制剂。灭活疫苗保留了抗原的免疫原性,当注射到机体体内后,灭活的病毒颗粒作为抗原物质,刺激机体产生抗体,从而使机体具有抵御该种(型)病毒的能力。目前国内已上市的七款新冠疫苗中,有五款为灭活疫苗,其中包括北京生物、武汉生物、科兴中维等。我们从专利中可以大致看出灭活疫苗的生产工艺。以北京生物为例,其在专利CN111662881B中公开了一种新型冠状病毒SARS-CoV-2的Vero细胞灭活疫苗病毒液的生产方法,包括在装填有片状载体的篮式生物反应器中加入细胞生长液,接种Vero细胞进行培养,至长成致密单层后,采用细胞维持液洗换;洗换结束后注入细胞维持液,进行新型冠状病毒的接种,病毒接种的MOI为0.005~0.4,病毒培养温度为36±1℃,溶氧≥40%,控制病毒培养阶段体系pH值为7.2~7.6;病毒接种后培养48~96h,收获病毒液。该方法应用篮式反应器成功培养获得了新型冠状病毒Vero细胞灭活疫苗病毒液,细胞接种密度大,病毒滴度高,批间差异高度可控且质量均一。其另一篇相关专利CN111575249B公开了一种新型冠状病毒SARS-CoV-2的Vero细胞灭活疫苗病毒液的纯化方法,包括将灭活的新型冠状病毒SARS-CoV-2的Vero细胞病毒液通过滤膜初步过滤,然后通过滤膜超滤浓缩得到新型冠状病毒浓缩液后加入核酸酶,降解Vero细胞中残留的DNA,之后将复合填料Capto Core 700装入层析柱中,先采用碱液冲洗,再用洗脱液平衡2~5个柱体积,接着将病毒浓缩液泵入到层析柱中,洗脱液洗脱;在紫外检测波长280nm条件下,收集第一个流穿峰即为病毒纯化液。该方法采用超滤浓缩、核酸酶消化和柱层析工艺步骤,结合复合填料Capto Core 700对新型冠状病毒液进行纯化,能够快速、稳定地大规模生产新型冠状病毒Vero细胞灭活疫苗病毒纯化液。从北京生物相关专利公开的内容可以发现,新冠灭活疫苗生产工艺大致为应用篮式生物反应器制备新型冠状病毒灭活疫苗(Vero细胞)病毒液,经过病毒培养、灭活、纯化,后经适当稀释后配制新型冠状病毒灭活疫苗,配制后分装,得到新型冠状病毒Vero细胞灭活疫苗制品。腺病毒载体技术简单来说就是把腺病毒中原有与复制相关的基因剔除,替换为新冠病毒刺突蛋白(S蛋白)的基因。这样做的目的是使重新组装的病毒复制新冠病毒刺突蛋白,从而刺激我们的免疫系统启动免疫应答,产生免疫记忆。目前国内上市的腺病毒载体新冠疫苗是由军事科学院军事医学研究院陈薇院士团队及康希诺生物联合研发的。康希诺相关专利CN111218459B中公开了制备重组腺病毒的方法:以E1、E3联合缺失的复制缺陷型人5型腺病毒为载体,以整合腺病毒E1基因的HEK293细胞为包装细胞系,携带的保护性抗原基因是经过优化设计的2019新型冠状病毒(SARS‑CoV‑2)S蛋白基因(Ad5‑nCoV),通过构建穿梭质粒载体、转染入宿主细胞、培养宿主细胞、收获宿主细胞中释放的人复制缺陷重组腺病毒、对重组腺病毒进行扩大培养、纯化等步骤来制备所需的重组腺病毒。该方法中S蛋白基因经优化后,在转染细胞中的表达水平显著升高,且疫苗制备快速简便,可在短期内实现大规模生产用于应对突发疫情。此外值得一提的是,10月26日,由康希诺研制的全球首款吸入用重组新型冠状病毒疫苗(5型腺病毒载体)(简称“吸入式新冠疫苗”)在上海正式开始免费接种,这款疫苗与其此前已经获得附条件上市批准的注射用新冠疫苗“克威莎”同属一款疫苗,在肌注型腺病毒载体新冠疫苗“克威莎”的基础上创新给药方式,用雾化器将疫苗雾化成微小颗粒,通过口腔吸入的方式完成接种。对于吸入式新冠疫苗,康希诺在专利方面“早有准备”,早在2020年8月24日康希诺就申请了给药方式为黏膜给药的SARS-CoV-2重组腺病毒载体疫苗相关专利(CN113750227A)并申请了PCT国际专利,随后更是布局了多件雾化装置相关专利(详见图3)。中国科学院微生物研究所与安徽智飞龙科马生物制药有限公司联合研发的重组蛋白新冠疫苗是我国首个获批的重组新冠病毒蛋白疫苗,是将新冠病毒最重要的抗原部分,放到一个工程细胞系里面来生产,然后将它生产出的抗原蛋白经过纯化,再与佐剂进行混合,最后接种到人体内。关于其生产工艺,智飞生物在专利CN113584106B中公开了一种CHO细胞表达的重组新型冠状病毒NCP-RBD蛋白的制备方法,包括取工作细胞株(表达重组新型冠状病毒NCP‑RBD蛋白的重组CHO细胞株)进行复苏培养,得到细胞复苏培养物后将细胞复苏培养物进行扩增,得到细胞扩增培养物,之后将细胞扩增培养物进行罐培养,得到细胞收获液,最后将细胞收获液进行纯化,得到所需产物。该方法可以将CHO细胞表达的重组新型冠状病毒NCP‑RBD蛋白高效的分离和纯化,适用于规模化生产,同时能有效地用于生产新冠疫苗。智飞生物关于重组蛋白新冠疫苗的制备方法,将最有效的抗原成份通过基因工程的方法,在体外细胞中表达,通过类似于工业发酵的方式(即生物反应器)来生产蛋白,经过纯化后制成疫苗,整个生产过程仅涉及蛋白表达和纯化,没有活病毒,因此生产过程安全性好,容易大规模生产。根据相关研究,目前灭活疫苗无法有效应对病毒突变,而mRNA疫苗在刺激细胞免疫方面具有一定优势,此外mRNA疫苗产业化容易、速度快、成本低,从基因测序至生产只需要数周的时间,因此在对时间要求比较紧急的疫情中有望发挥重要作用。此外,mRNA技术在理论上可以生产出任何一种人类所需的蛋白质,在传染性疾病以外的领域应用前景也非常广阔,由此可见,mRNA技术的价值是不言而喻的,是未来各国相关企业的研发重点。虽然目前国内尚无mRNA 新冠疫苗获批,但在新冠mRNA疫苗赛道上,超10家药企已有相关产品研发和专利布局,例如沃森生物、艾博生物、斯微生物、艾美疫苗、深信生物、威斯津生物、康希诺、石药集团、蓝鹊生物、复星医药等。然而,mRNA技术存在两大关键技术难点:序列设计和递送系统,其中mRNA序列结构决定抗原蛋白结构、免疫原性及稳定性,优秀的序列设计可以更高效地表达抗原蛋白,最终提高mRNA疫苗激活特异免疫的精确性和活性。而递送系统是目前产能扩张的瓶颈,也是目前mRNA疫苗的主要研发壁垒。由于mRNA很难通过细胞膜表面的脂质双分子膜层以及mRNA具有的高天然免疫原性,其在体内传递效率低下,难以高效率地发挥作用,因此要实现mRNA疫苗的广泛应用,高效的递送系统是关键。在递送系统方面,主流方法是采用LNP(脂质纳米粒)技术递送,LNP将mRNA包载其中,保护mRNA免于递送过程的酶降解和免疫系统的清除,提高mRNA体内稳定性,促进其跨膜转运且在细胞质中释放mRNA用于翻译蛋白,蛋白刺激机体产生免疫反应从而实现机体免疫。目前,国际公认的mRNA巨头公司分别是Moderna、BioNTech和CureVac。但LNP技术的专利却并不属于这三家公司,LNP技术专利最开始由加拿大生物药企Arbutus所掌握,曾授权给Moderna、CureVac和BioNtech。后来Moderna选择自主研发,只不过Moderna在与Arbutus的LNP专利纠纷中败诉,而BioNTech及CureVac在mRNA疫苗中使用的LNP载体,则明确是来自Arbutus的专利授权。针对LNP递送技术,Arbutus申请了多项针对性的保护专利,其LNP递送系统的核心专利US8058069B2(中国同族专利为CN102119217B)保护范围包含核酸、阳离子脂质、非阳离子脂质、缀合脂质以及各成分的比例,对LNP组合物的组份及其配比进行了非常全面的保护,在2029年专利到期之前难以撼动。
图4 Arbutus的LNP递送系统核心专利
由于LNP的专利难以突破,如果企业不想通过授权使用,只能从发起专利挑战或规避设计方面做文章,规避设计如采用区别于专利中阳离子脂质体的脂质或通过改变各组分配比实现优化,以寻求绕过现有专利的可能。目前,许多国内相关企业也想突破国外企业的专利壁垒,采用改进的LNP,并且已经开始布局相关专利,其中深信生物于2020年8月申请了相关专利“一种脂质纳米颗粒”(CN114073677A),艾博生物于2021年8月申请了相关专利“脂质化合物和脂质纳米颗粒组合物”(CN114391008A),康希诺与键凯科技于2022年1月申请了相关专利“一种用于核酸递送的新型可电离脂质及其LNP组合物”(CN114149337B)并获得授权。这种方法理论上可行,但真正能投入使用可能还需要一定时间。此外值得一提的是,与现阶段大部分企业都采用的LNP递送系统不同,斯微生物采用LPP递送系统,由其联合创始人沈海法研发,巧妙地绕开了LNP结构专利,并于2017年获得美国休斯顿卫理公会医院LPP递送平台全球独家商业化授权。据斯微生物官网介绍,LPP (lipopolyplex) 纳米递送平台是一种以聚合物包载mRNA为内核、磷脂包裹为外壳的双层结构,LPP的双层纳米粒和传统的LNP相比具有更好的包载、保护mRNA的效果,并能够随聚合物的降解逐步释放mRNA分子,LPP平台优异的树突状细胞靶向性可以更好地通过抗原递呈激活T细胞的免疫反应,从而达到理想的免疫治疗效果。综合来看,国内相关企业已具备专利预警和避开专利壁垒的前期意识,同时正凭借自身研发能力布局具有自主知识产权的关键专利技术,国产新冠疫苗竞争力进一步加强,在未来新冠疫苗领域的全球竞争中,中国企业有望占据更有利的地位。作者:朱江月 品源知识产权代理















 首页
首页 电话咨询
电话咨询 联系方式
联系方式






